RESEARCH
長い旅をしてできる血管内皮細胞
脊椎動物の胚発生で見られる体節は、将来、筋肉や骨格になることがよく知られています。からだの前後軸に沿った節構造をもつ体節を作り出すには、Notchシグナルによる細胞間コミュニケーションが重要であることを見いだしました。さらにその後もNotchシグナルは、形成された体節の一部の細胞で働き続けていることに気がつきました。この細胞を追いかけたところ、体節の腹側に位置する背側大動脈まで動いていき、そこで血管内皮細胞になっていました。長い道のりを旅して血管になる細胞を特定できたのです。
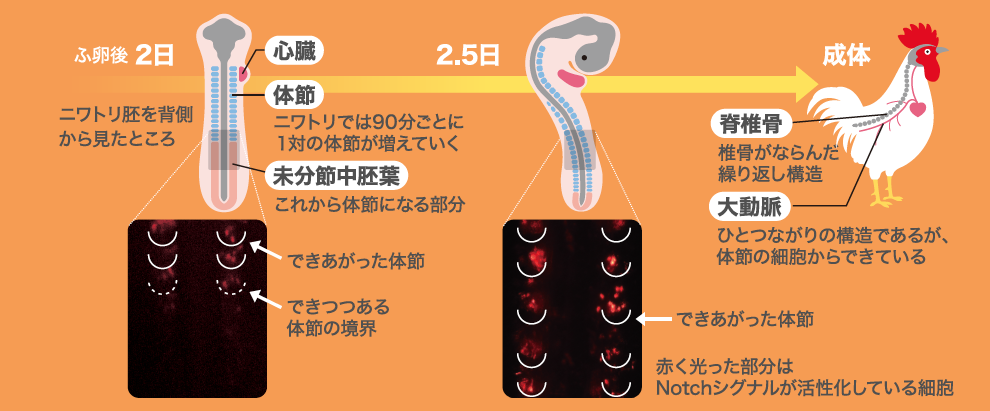
1.Notchシグナル活性化細胞のゆくえ
体節は「大切」である。発生生物学用語の体節が、「大切」と同じ発音なのは、私にとって単なる駄洒落を超えた意味深さがある。そう感じたのは、ニワトリ胚で脊椎動物の体節形成メカニズムの研究を始めて5年目のこと、体節の中から血管内皮細胞を分化させるしくみを発見した時である。体節は、全ての脊椎動物の胚の体幹部において一時的にみられる繰り返し構造であり、将来、真皮や筋肉、骨などをつくりだす。われわれのからだがしなやかな動きをできるのは、背骨や筋肉が体節の分節構造をもとにしてできているからである。体節は、発生初期に未分節中胚葉と呼ばれるひとつづきの組織が、前から順に規則的に分断されてできる。私は、体節を切り分ける境界を作り出すしくみを明らかにしたいと考えて研究を始めた。そして、隣り合う細胞間の情報伝達を担う機構のひとつ—Notchシグナル(註1)—によって境界が決まることを見いだした。このシグナルは、体節の分節化の際にだけにはたらき、体節ができてしまえばその役割を終える…ということであれば、話は単純だったのだが、体節ができたあとも体節の後ろ側半分で活性化し続けていた。このNotchシグナル活性化細胞は、その後どのようにからだづくりに関わるのだろうか?という新しい疑問が生まれたのである。
(註1)Notchシグナル
細胞膜の表面に出ているNotch受容体は、隣に接している細胞の表面上にあるリガンド(Deltaなど)と結合すると、それが刺激となって、 活性化し、細胞内へ情報を伝える。Notchシグナルは、細胞内のネガティブフィードバック経路を巧みに利用して、隣り合う細胞間に違いを生み出す情報伝達機構であることがよく知られている。神経細胞の分化誘導時にみられる側方抑制現象は、Notchシグナルによる分化制御の代表的な例である。
2.体節細胞から血管内皮細胞へ
Notchシグナル活性化細胞の行方を追うと、体節から抜け出して、背側大動脈で血管内皮細胞になっていた。そこで、体節細胞で人為的にNotchシグナルを活性化させたところ、もともと血管になるはずのない細胞も、背側大動脈の血管内皮細胞に分化してしまった。逆にNotchシグナルを抑制すると、体節細胞は血管内皮細胞にならない(図1)。つまりNotchシグナルが体節細胞を血管内皮細胞へと分化させるスイッチとしてはたらいているのである。これまでの研究から、Notchシグナルは隣り合う細胞同士をそれぞれ異なる細胞へと分化させる時に働く細胞間情報伝達機構であることが知られている。ほとんどが筋骨格系の細胞に分化する体節の中で、血管内皮へと分化するほんのわずかな細胞を適正に「仕分け」する役割を、Notchシグナルが担っているのだろう。背側大動脈は、最初に血流循環が始まる血管であり、胚性血球分化(註2)の担い手でもあって、将来は大動脈になる。血管ワールドでは主役級のプレーヤーだ。体節と背側大動脈という胚発生の初期に隣接する位置関係にあるキープレイヤー同士をつなぐNotchシグナルの役割を明らかにすることができた。成体では、独立した機能を発揮する組織同士だが、胚発生過程では関わり合いながら、それぞれに固有のかたちを作っていくのである。
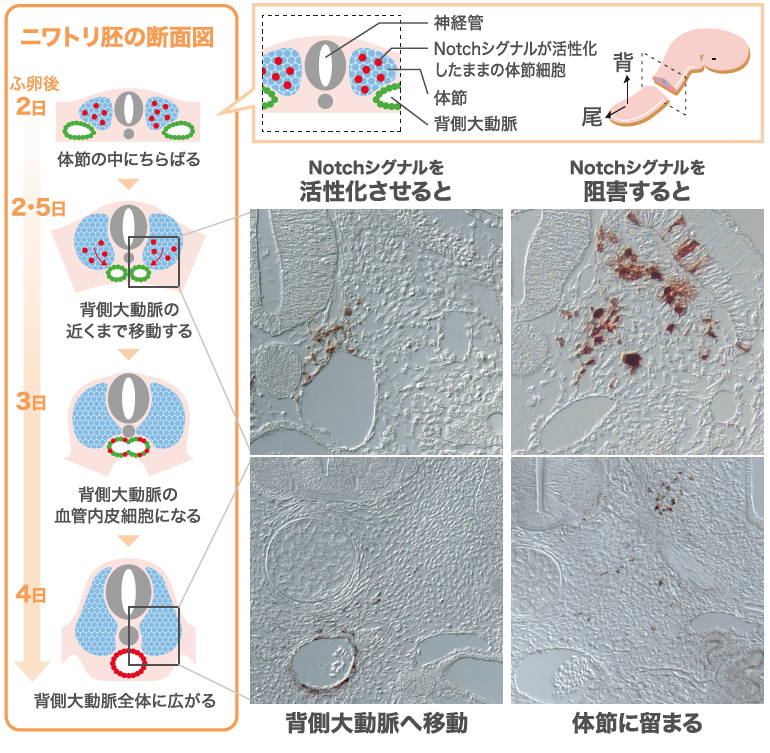
(図1) 背側大動脈まで移動する体節細胞
Notchシグナルが活性化された体節細胞はふ卵開始後2.5日目には背側大動脈の近くに集まり、4日目には血管内皮細胞になる。一方、Notchシグナルをうまく伝えられなくした体節細胞はその場にとどまり背側大動脈へ移動しなかった。
(註2)胚性血球分化
成体では、骨髄幹細胞から生まれる血球細胞だが、骨髄ができる以前の発生期には、他の組織から生まれる。背側大動脈も発生の一時期において、自身の血管内皮細胞の一部から血球細胞を作りだす役割を担っている。
3.体節が追い出し、血管が呼び寄せる
Notchシグナルが活性化された体節細胞は、通常の体節細胞が有することのない特別な移動能力を獲得している。この細胞だけが体節内を通り抜けて背側大動脈へまで移動するのである。いったん背側大動脈近くにまで移動したNotch活性化細胞を、背側大動脈から最も遠い位置の体節内へ移植してみても、あたかも自分がたどりつくべきゴールを知っているかのように、数時間後には200μm以上もの厚みがある体節を通り抜けて、背側大動脈へと移動している。この移動のしくみを知るために、Notchシグナルが活性化した体節細胞で特異的に発現が上昇する分子をさがしたところ、エフリンB2という膜に局在するリガンド分子が候補として上がった。エフリンB2分子を膜にもつ細胞は、その受容体(何種類もあり、Eph受容体と総称される)を膜にもつ細胞と出会うと、双方の細胞内へ情報を伝え合い、互いを遠ざけあう力(細胞間反発力)が発生することが知られている。
そこで、エフリンB2がはたらかないように細胞を操作してみると、Notchシグナルが活性化していても体節にとどまり続けて血管内皮細胞にはなれないことがわかった(図2)。つまり、体節の細胞が背側大動脈へ移動するには、エフリンB2が引き起こす細胞間反発力が必要なのである。次に知りたいのは、エフリンB2によって体節に別れを告げることができた細胞たちが、目指すべき背側大動脈の位置を知る機構である。もし、背側大動脈が何らかの誘引因子を放出して、細胞を導いていれば、彼らは迷わずそこへたどり着けるはずである。この仮説を検証するため、ある胚から取り出した背側大動脈を、別の胚の背側大動脈ができる場所とは反対の位置へ移植し、Notchシグナルを活性化した体節細胞がそちらへ引き寄せられるかどうかを調べた(図2)。その結果、Notchシグナル活性化細胞は、見事に移植された背側大動脈の側へ移動した。つまり、背側大動脈が誘引シグナルを発して、体節細胞を導いているのである。エフリンB2とその受容体による細胞間反発力と背側大動脈からの誘引作用とのはたらきで、体節の細胞は背側大動脈へと移動できるのである。ただし、背側大動脈が分泌している誘引分子は、未だ謎のまま残されている。
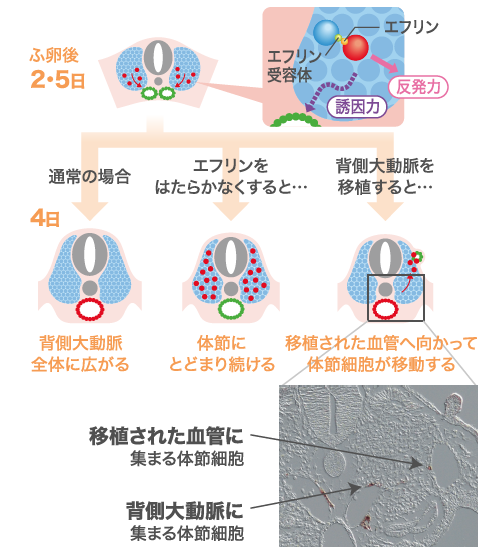
(図2)体節から追い出すエフリンと引き寄せる背側大動脈
エフリンをはたらかなくした胚ではNotchシグナルが活性化した細胞は体節に残り続けた。背側大動脈を別の胚に移植すると、Notchシグナルが活性化した細胞が引き寄せられた
4.体節の後ろから出る血管、前から入る神経
分節化をきっかけにして、体節の前側半分と後側半分は、それぞれ異なる性質をもつようになる。体節の前後の区画ができる際にNotchシグナルがはたらいていることは、マウス胚やゼブラフィッシュ胚の研究から明らかにされていた。ニワトリ胚を用いた我々の実験でも、Notchシグナルが活性化した細胞は体節の後半部分だけに集まり、Notchシグナルが阻害された細胞は体節の前半部分へと集まるという特徴的な性質を示した(図3)。このことからNotchシグナルは、まず体節の境界を決め、次に体節の前半と後半の細胞の性質の違いを生み出し、その後、体節の後側部分から背側大動脈へと血管になる細胞の移動を引き起こす、という順序で働いていることがわかった。実は、体節の前側は神経堤細胞(註3)が移動し、そこで背側神経節がつくられることが以前から知られている。体節の後側細胞はエフリンB2他、複数のエフリンを、神経堤細胞はEph受容体のいくつかを発現しており、これらの分子を介した両者の反発により、神経堤細胞は体節の前側だけに移動するのである。今回の我々の実験で、体節の後側では、Notchシグナルとその下流ではたらくエフリンB2によって、一部の細胞が血管内皮細胞となるために背側大動脈へと移動することがわかった。つまり、血管と神経は、体節が作り出す秩序に従って、それぞれのふるまいを決めているのである(図4)。体節の秩序を作り出すために使われる分子群は、NotchシグナルやエフリンーEph受容体など、驚くほどに少ない。しかもこれらは、体節形成だけでなく血管や神経のパターニング過程で何度も繰り返し登場してくる。胚の発生現象ではその場その場で限られた遺伝子をうまくやりくりし、複雑なかたちを作り出しているようである。
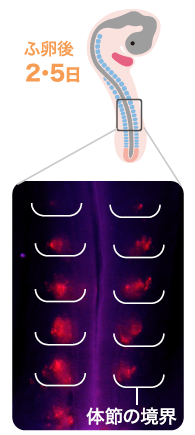
(図3) 体節の前半と後半の性質を分けるNotchシグナル
人工的にNotchシグナルを活性化した細胞(赤)は体節の後半に偏っていた。
体節から血管内皮細胞を作り出すというNotchシグナルの新しい役割を見つけることができたのは、「大切な体節」の本来の機能を損なわない程度に、特定の発生時期の体節へ遺伝子導入実験ができ、その影響を細胞レベルで追跡できたからである。このような実験は、ニワトリ胚ならでは(註4)。ニワトリ胚を使って新しい血管形成のしくみを導きだしたことで、モデル動物としてのニワトリ胚に魅了されてしまった。
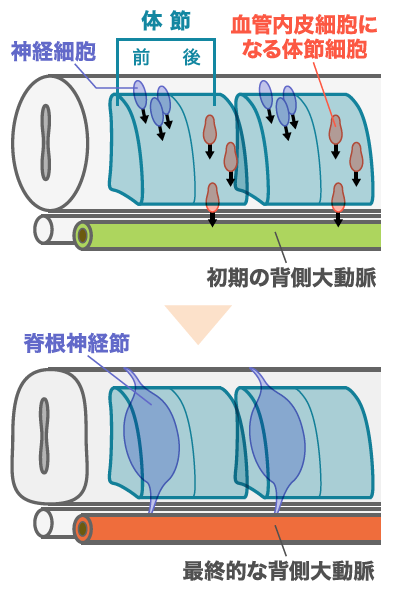
(図4) 体節の前から入る神経と後ろから出る血管内皮細胞
(註3)神経堤細胞
神経堤細胞は神経管の背側の一部から生まれ、神経管から離れた場所まで移動しして、脊髄神経節、交感神経節、腸管神経、色素細胞、頭蓋骨などの多岐にわたる組織・器官を作り出す。
(註4) ニワトリ胚ならでは
遺伝子がもつ電荷を利用して、電気刺激によって細胞内へ遺伝子を導入する技術(エレクトロポレーション)を用いると、特定の細胞群に遺伝子を導入できる。導入する遺伝子のデザインを工夫すれば、目的の遺伝子を発現させる時期の調節等も可能である。したがって、胚発生で繰り返し使われるような遺伝子についても、注目する時期に的を絞って解析を行うことができる。
5.血管内皮細胞は動き続ける
ニワトリ胚に惚れ込んだ私であったが、現在はウズラ胚をモデル動物として、血管の形成メカニズムの研究を行っている。ウズラは、卵も成体もニワトリと比べて小さい分、系統の維持や卵の保管が容易な上に、孵化や性成熟までの期間がマウスに匹敵するくらい短いため、遺伝学的な研究手法を取り入れることが可能だからである。血管内皮細胞が長い距離を移動して血管を作ることを見いだした以上、そのメカニズムとそれがもつ意味を知りたい。そのためには、経時的な観察を行い、血管を作る個々の細胞の挙動を観る必要がある。そこで、「血管が光るトランスジェニックウズラ」を作った(註5)。血管内皮細胞だけで活性化する遺伝子を利用して、蛍光タンパク質を光らせる。蛍光タンパク質は細胞の核だけに留まるようデザインしてあるので、生きたままの胚を培養しながら共焦点レーザー顕微鏡でからだの深部にある細胞の動きを経時的に観察できる。その画像をコンピューター解析にかければ、血管内皮細胞すべての位置の変化を正確に追跡できる。こうして、ウズラ胚の体内で血管ができあがっていく過程が、四次元(三次元情報+時間変化)的にわかる(動画1)。現在、このウズラ胚を使って、どれだけの数の細胞が、どれくらいの速さで、どのような軌跡を描きながらどこへ向かっていくのか。そして、それらの動きは周囲の組織の形態形成とどのように協調しあって、機能的な血管のネットワークパターンを作り上げるのかを明らかにしようとしている。複雑な現象ではあるが、観察をするたびに新しい発見があり、長年見てきたはずの鳥類の胚なのに、まだまだ知らないことばかりなのだと、常に新鮮な気持ちになっている。
(動画1)血管内皮細胞の核が光るウズラ胚
腹側から見た左右に二本の背側大動脈が正中線に向かって少しずつ移動する様子がわかる
(註5)血管が光るトランスジェニックウズラ
トランスジェニック鳥類の作製は、他のモデル動物のトランスジェニック作製法と比較するとたいへんな手間がかかる。血管のイメージング解析を見据えたトランスジェニックウズラの作製は、筆者の前所属研究室(カリフォルニア工科大学Scott E. Fraser教授)のRusty Lansford博士がプロジェクトを立案・先導し、2名のテクニシャンが2年がかりで系統を樹立した結果可能になった。苦労の賜である。
佐藤有紀(さとう・ゆき)
熊本大学大学院先導機構特任助教。1998年北里大学理学部卒業。2003年奈良先端科学技術大学院大学バイオサイエンス研究科博士課程修了。理化学研究所発生・再生科学総合研究センター、カリフォルニア工科大学バイオイメージングセンターの研究員を経て2009年より現職。
![[科学のコンサートホール]BRH JT生命誌研究館](/common/img/logo.svg)