顧問の西川伸一を中心に館員が、今進化研究がどのようにおこなわれているかを紹介していきます。進化研究とは何をすることなのか? 歴史的背景も含めお話しします。
バックナンバー
水平遺伝子伝搬
2014年6月16日

皆さんはTALEN(ターレン)やCRISPR(クリスパー)について聞いたことがあるだろうか。実は生きた細胞の中でゲノム遺伝子を編集するための新しい技術として今世界中で大流行りの技術だ。図1に概要を図示しているが、CRISPRは1987年大阪大学中田さん等のグループの発見をきっかけに開発された遺伝子操作技術で、CAS9と呼ばれる蛋白が、ホスト遺伝子に結合する短いガイドRNAを認識し結合部位を切断する性質を利用している。高い効率でゲノム遺伝子を編集することが出来るため、遺伝子ノックアウトを始め様々な動物の遺伝子編集に使われている。
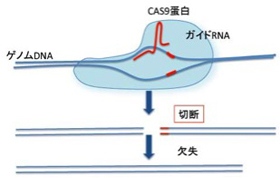
図1 CAS9蛋白とガイドRNAを利用した遺伝子編集
CAS9蛋白はCRISPR系に属する一つの蛋白で、ヘアピン構造をとるガイドRNA(図では赤いU型の構造)に結合する。ガイドRNAのもう片方はホストDNAに結合することで、CAS9蛋白をゲノムの標的部位にガイドしてくる。CAS9蛋白はガイドされた場所のDNAを切断する。これを利用して様々な遺伝子編集を行う。
最近の例を紹介すると、サルの受精卵にCAS9蛋白とガイドRNAを導入して発生させると、生まれて来た子供の3割に望み通りの遺伝子改変が可能だったという結果が中国の研究グループにより示されている。これまで遺伝子ノックアウトなどは実験系が整備されたモデル動物でしか可能でなかったが、今後は様々な動物で遺伝子編集が容易になるだろう。これから少なくとも10年はCRISPR時代が続くと思っているのは私だけではないはずだ。この様な効率の高いゲノム遺伝子改変を可能にするCASファミリー分子は実に9割の古細菌に保存されているが、この分子の本来の機能は、侵入したウィルスなどの外来DNAを破壊する巧妙な系だとわかっている(図2)。例えばCRISPRを持つ細菌にウィルスなどのDNAが侵入すると、決まった長さにカットされ、その一部がホストゲノムにあるCAS遺伝子群が集まるCRISPR部位に速やかに加えられて行く。CRISPR部位ではホストゲノムに組み込まれた外来遺伝子は常に転写されRNAに変換される。このRNAが新たに侵入した外来遺伝子にCAS分子を案内し外来のDNAを特異的に破壊する。一種の免疫記憶に関わるメカニズムといえる。
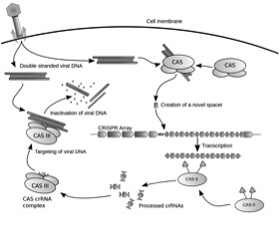
図2 外来遺伝子の侵入を防ぐCRISPR系
CRISPR部位には幾つかのタンパク質遺伝子と、短い転写されRNAとして機能する部分が集まったクラスターを形成している。ウィルスが侵入すると、そのDNAは小さな断片にカットされる。その一部がCRISPRクラスターに取り込まれ、ガイドRNAとしての役割をはたす。次にウィルスが入ってくると、このガイドRNAがCAS蛋白をウィルスのDNAにガイドしてウィルスDNAを分解する。これにより更なるウィルスDNAの侵入、増殖を防ぐ。(作図:James atmos)
ただこのことを裏返せば、細胞が常に外来のDNAの侵入に悩まされていることを意味している。事実外来遺伝子の侵入を防ぐCRISPRだけでなく、ゲノムに入り込んだ外来遺伝子を不活性化するための様々な仕組みはほとんどの生物に広く認めることが出来る。この様に外来の遺伝子が入って来てゲノムに取り込まれることを水平遺伝子伝搬と呼ぶ。細菌全体が内部寄生しなくとも、遺伝子の一部が水平伝搬されるだけで、以前にはなかった遺伝子、あるいは遺伝子群を一度に導入し、新しい機能を手に入れることが出来る機構だ。事実、CRISPR遺伝子群もおそらく水平伝搬で拡がったのではと考えられている。
ウィルス感染による遺伝子の水平伝搬は私たち人間でも普通に起こっている。例えばレトロウィルスに感染すると、そのウィルスが持っている全ての遺伝子が私たちのゲノムの中に組み込まれる。更にこのウィルス遺伝子が宿主遺伝子の一部を取り込んで他の細胞に感染することもある。この場合はウィルス遺伝子だけでなく、細胞ゲノムの一部が細胞から細胞へ移行する。この時取り込んだ遺伝子に変異が起こり発がん性を持つことがある。こうして一部の発ガンウィルスが出来たと考えられる。現在ではこの様なレトロウィルスの水平伝搬能力を利用して、目的の遺伝子を細胞に導入するためのツールとして使われている。山中iPSが最初作成されたときは、このレトロウィルスによる遺伝子伝搬を使って作成された。
しかし水平伝搬はウィルスだけに媒介されるわけではない。特にゲノム研究が進んだ結果、共生関係にある多細胞動物と細菌については遺伝子の水平伝搬が広く見られることがわかって来た。原核生物が内部共生してミトコンドリアが進化したように、細菌が多細胞動物と内部共生を行っている例が昆虫では数多く見つかっている。アブラムシに見られる、菌を自分の中で培養している恐るべき菌細胞については季刊生命誌で石川さんが詳しく紹介された。ミトコンドリアの多くの遺伝子が宿主の核に移行したように、内部共生は異なる生物間の遺伝子交換が起こるメカニズムとして多細胞動物にも広く存在しているようだ。ただ多細胞動物になると身体の細胞が、精子や卵子などの生殖細胞とそれ以外の体細胞に分かれている。子孫には、生殖細胞のゲノムからしか遺伝子は伝わらない。しかし、細菌によっては生殖細胞を好んで宿主にする細菌がある。ボルバッキアだ。
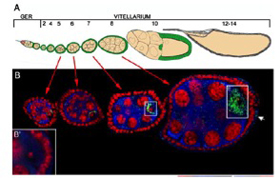
図3 ショウジョウバエ卵形成過程とボルバッキアの局在
緑でマークされているのがボルバッキア。将来の卵子に強く濃縮されていることがわかる。Ferree PM et al, Wolbachia utilizes host microtubules and dynein for anterior localization in the Drosophila Oocyte. 2005 PlosPathogen, 1: 0111
図3はショウジョウバエの卵巣を示しているが、ボルバッキアは卵子に濃縮されているのがわかる。ではこの様な細胞の中で遺伝子の水平伝搬は起こっているのか。この問題に最初に挑戦したのが産総研の深津さん達のグループだ(PNAS 99, 14280-14285, 2002)。この研究では、図3に示したショウジョウバエと同じように卵子にボルバッキアが寄生し子孫に伝わるアズキマメゾウムシが使われている。ボルバッキアを卵子から駆除しようと抗生物質処理をしてもボルバッキア遺伝子がいっこうに消えないという問題に直面したグループが、消えない原因がひょっとしてボルバッキア遺伝子が宿主のゲノムに水平伝播したのではと気づいて始まった研究のようだ。水平伝搬していれば遺伝子にボルバッキア遺伝子があるはずだと、アズキマメゾウムシのゲノムを調べた結果4.1Kb,11.4Kbのボルベッキア遺伝子断片がアズキマメゾウムシのX染色体に水平伝播していることを突き止めた。おそらくこの研究は、内部共生関係から遺伝子水平伝達が起こることを証明した初めての論文だろう。その後、ヒトゲノム解読で有名なベンターが設立した研究所のホトップ(Dunning Hotopp)が2007年様々な昆虫や線虫のゲノムのなかにボルバッキアゲノムが紛れ込んでいないか大規模に調べサイエンス誌に発表した(Science 317, 1753-1755, 2007)。驚くべきことに4種類の昆虫、4種類の線虫にボルバッキア遺伝子の水平伝搬が確認された。データベースの検索からも更に3種類の昆虫ゲノムにボルバッキア遺伝子が混じっていることが確認された。深津さん達の実験ではボルバッキア遺伝子が昆虫細胞で発現していることは確認できなかったが、ホトップらはゲノムに伝搬したボルバッキア由来遺伝子が細胞の中で転写されていることも明らかにした。このことからわかるのは、生殖細胞へ内部共生を介して遺伝子が水平伝搬する現象は、多細胞生物に広く見られ、全く違った生物から新しい機能を持った遺伝子を丸ごと獲得することも生物の進化に役立っている可能性だ。特にホトップらの論文は、ショウジョウバエのある種にはボルバッキアゲノムがほぼ丸ごと組み込まれていることも示している。ミトコンドリアや葉緑素の場合は機能を持った構造として内部共生細菌の名残をみることが出来るが、形はすっかり消えても遺伝子情報だけがそっくり乗り移って宿主になりきっている例があるのを見ると、リン・マーギュリスが予想したように真核細胞にしかない有糸分裂なども様々な生物から遺伝情報を集めて生まれたのかもしれないと思う。進化では種が分離する過程を研究するが、分離しても生物同士で情報の交換を行うことが出来る。本当に地球上の生命は同じ家族だ。
※8月23日(土)日本進化学会第16回大阪大会 サイエンストーク&シアター(入場無料・要整理券)にて、深津武馬さんの講演があります。最新の研究成果をもとにわかりやすくお話ししていただけます。共に生きることの本質をぜひ一緒に考えましょう。
![[科学のコンサートホール]BRH JT生命誌研究館](/common/img/logo.svg)