年度別活動報告
年度別活動報告書:2008年度
脊椎動物の頭部神経はどのように部域化されるのか
橋本主税(主任研究員) 阿草耕介(研究スタッフ)
阿草耕介(研究スタッフ)
村戸康人、川辺実季(大阪大学大学院生)
はじめに
脊椎動物のかたち作りを見て行くと、咽頭胚の形が種を超えて高度に保存されていることが分かっており、咽頭胚を形づくる機構に脊椎動物において普遍的な仕組みがあると考えられる。それまで全く異なる発生様式をとって来た胚が原腸形成を経て神経胚に至る所では互いに良く似た形態を示すことから、咽頭胚を形づくる上で最も重要な時期は原腸形成期であると予想される。実際に、原腸形成期において機能的に相同な領域には相同な遺伝子の働きが必要とされることが分かっており、脊椎動物の体づくりを一義的に決定しているのは原腸胚期であることは間違いない。
私たちは、脊椎動物のかたち作りを知るためにアフリカツメガエルを実験材料として咽頭胚のパターンがどのように出来上がるのかについて研究を行なっている。今年度に行なった研究としては、第一に、脊椎動物と原索動物を決定的に分ける意味での頭部構造を形づくる上できわめて重要な感覚器プラコードの形成機構に関して、第二に、ミトコンドリアに局在し細胞内環境の制御に働くと考えられているUCP2遺伝子が神経の形成にどのように関わるのかに関して、第三に、ツメガエルの胚発生過程を三次元デジタル情報として切り出しその情報から発生過程を詳細に解析する方法の開発に関して、以下に紹介する。また、今年度から新たに開始した研究としてツメガエルとイモリの発生様式の差異に関する研究についても最後に簡単に触れる。
結果と考察
(1)レンズプラコードはどのように決められるのか?
本研究の目的は、プラコードから生じる頭部感覚器官の形成を指標として、Xhairy2がプラコードの生成に果たす役割を明らかにすることである。脊椎動物の頭部は多種多様な組織・器官から構成される極めて複雑な構造体であり、この多くの部分が、プラコードと神経堤という二つの特殊な細胞集団から形成される。たった二種類の前駆細胞からこのように多様な細胞種が生み出されるという事実は、プラコードと神経堤における分化制御の重要性を物語る。しかもプラコードと神経堤は、脊椎動物に近縁であると考えられている頭索類や尾索類には存在が確認されていないため(Schlosser 2005)、脊椎動物を定義づける重要な組織であると言え、系統進化の観点からも非常に興味深い対象である。プラコードと神経堤はいずれも外胚葉の一部であるが、表皮領域と神経領域の境界という、本来組織として定義され得ない部域から形成される(Schlosser 2008)。脊椎動物の発生において重要な機能をもつ遺伝子が、アフリカツメガエル胚から数多くクローニングされてきたが、そのうち、bHLH転写抑制因子をコードするHesファミリーに属するXhairy2が、確認されている限りこの境界領域で最も早くから明瞭な発現をすることが分かっている。全てのプラコードが、この境界領域のうちのpre-placodal ectoderm (PPE)から生じると考えられおり(Streit 2004)、興味深いことにXhairy2の境界発現はPPEを含んでいる。
Xhairy2を機能阻害したオタマジャクシ胚の頭部を形態学的に解析したところ、網膜は正常なものの、水晶体(レンズ)の顕著な形成不全が明らかになった。脊椎動物の眼は、その構成要素を大きく網膜とレンズに二分することができる。網膜は間脳の一部に由来するが、レンズは近接するプラコードから形成される。この結果から、Xhairy2がレンズの形成に重要であることが示唆される。そこで、発生をさかのぼり、尾芽胚期におけるマーカー遺伝子の発現変化を指標にして、Xhairy2とレンズ形成の関係を解析した。Xhairy2を機能阻害しても、網膜系譜特異マーカーであるrx1やsix6の発現に顕著な変化は見られなかったが、レンズ決定マーカーであるL-mafや分化マーカーであるg1-cryの発現が顕著に減少した。頭部感覚器官の運命決定は神経胚期に起こる。眼に関しては、神経領域内の予定網膜領域からシグナルが発せられ、それを受けたPPE内の限られた領域でレンズ運命の誘導が起こりlens field (LF)が形成される。LFのマーカー遺伝子pax6などについて、Xhairy2機能阻害の影響を確認したところ、LFの発現が特異的に減少したが、網膜系譜の発現に変化は見られなかった。これは形態レベルでの結果と矛盾しない。
これまでの結果は、Xhairy2がレンズの形成に特異的に必要とされることを十分に示す。次に、このメカニズムについて解析した。まずレンズ誘導に関わることが知られているシグナル経路について、その構成因子の発現変化を確認したところ、既知のシグナル経路構成因子の発現には顕著な変化が見られなかったため、Xhairy2を過剰発現させてもLFの拡大が起こらないことと、Xhairy2が転写抑制因子であることを考慮し、Xhairy2機能阻害で発現が上昇ないし異所発現する遺伝子群に着目した。なかでも、p27xic1は、Xhairy2の下流で神経堤の形成に深く関わっていることが過去に明らかになっており(Nagatomo and Hashimoto 2007)、LFマーカーであるpax6と発現領域が重複せず相補的な位置関係にある。実際、Xhairy2を機能阻害すると、後期神経胚期に、p27xic1の異所発現の傍証となるアポートシスの誘導を見ることができる。p27xic1を過剰発現させると、LF形成に関してXhairy2機能阻害と同等の表現型が得られ、さらに、Xhairy2 機能阻害による表現型は部分的にp27 の同時機能阻害により緩和された。これらの結果から、Xhairy2によるp27xic1の抑制が、LFの形成に必須であることが示唆された。
p27xic1は、G1/S期の移行を阻害することで細胞周期を停止させることが知られている(Besson et al. 2008)。この特質から、Xhairy2機能阻害胚で見られるレンズ表現型、特にLFの消失は、遺伝子発現制御や細胞の性質転換などによらず、レンズ系譜前駆細胞の激減が原因であると推測できる。そこで、Xhairy2機能阻害胚において、 in situ共役のBrdU取り込みにより、LFないしそれに相当する領域での増殖能を調べたところ、神経胚の後期では確かに増殖能は低下していたが、LF誘導の時期である神経胚中期では、顕著な変化は見られなかった。また、薬剤処理により細胞周期を一定期間停止させた上で、LF形成ならびに球状レンズ形成を確認したが、顕著な変化は見られなかった。以上の結果から、Xhairy2はなんらかの形で細胞周期の制御に関わっているかもしれないものの、Xhairy2機能阻害胚で見られたLF消失の表現型は、レンズ系譜細胞の単純な減少によるものではないことが示唆さた。興味深いことに、p27xic1は細胞周期の制御と独立して分化を誘導する活性を有することも知られている(Vernon et al. 2003)。一アミノ酸の置換によって細胞周期阻害活性を失ったp27xic1の変異体を過剰に発現させても、野生型と同じようにXhairy2機能阻害の表現型を模倣するような結果が得られる。この問題の分子機構をより明確に解くには今後一層のきめ細やかな実験が必要とされるが、今回の一連の検証によってXhairy2とp27xic1の関係による分化状態の制御の関連が浮き彫りになったと言える。
さて、プラコードや神経堤は、その運命が最初に指定されてから実際に分化が開始されるまでにかなりのタイムラグがある。この期間、如何にして組織幹細胞様の未分化性を維持できるかが極めて重要であることは間違いない。レンズ形成を指標にしたとき、Xhairy2が転写因子カスケードの最上流に位置するわけではなく、尚かつp27xic1の発現抑制を介して分化抑制に関与していることから、Xhairy2がPPEで先行して発現することで未分化性が積極的に維持されているのではないかと考えられる(図1)。シグナル入力から始まる分化のカスケードは、この基本的な細胞の状態、コンピタンスがベースとして存在して初めて、正常に機能するのではないかと考えられよう。
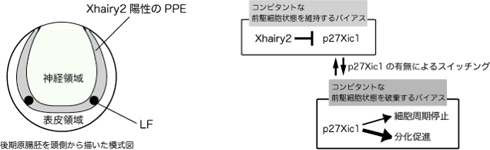
図1 LFが形成されるPPEには、Xhairy2が存在することで前駆細胞状態を適切に維持するバイアスがかかっている。
(2)初期発生におけるミトコンドリアタンパク質UCP2の発現パターンおよび役割を探る
脊椎動物の脳は終脳・間脳・中脳・後脳といった領域に分かれているが、これらは脳の構造ができる前の発生の非常に初期の段階(初期神経胚)で決定されている。この領域の決定にはさまざまな転写因子が関わっており、それらが領域特異的にカスケードをつくることで各領域が特徴づけられる。このことから脳の領域決定においては転写因子が各領域のマーカー遺伝子として非常によく研究されている (Sasai, 2001) (Wigle and Eisenstat, 2008) 。
ミトコンドリア内膜タンパク質であるUCP2(uncoupling protein 2)はATP産生の調節や活性酸素種の産生を抑制する (N?gre-Salvayre et al., 1997)ことなどが知られており、これまで主に哺乳類の成体や培養細胞におけるエネルギー代謝やそれに派生する細胞の機能に関わる研究がなされてきた (Joseph et al., 2004) (Yamada et al., 2006)。
UCP2の発現パターンをアフリカツメガエルの初期胚においてRT-PCRおよびwhole mount in situ hybridization法を用いて時間的・空間的に観察したところ、非常に興味深い結果が得られた。当初、ミトコンドリア内膜タンパク質であるUCP2はどの細胞でも常に発現していると考えられた。しかし解析の結果、将来中枢神経となる組織が形成される初期神経胚では、UCP2は神経領域の中でも特に予定後脳の第3・第4・第5分節および将来眼となる領域に強い発現が見られた。さらに初期尾芽胚では予定後脳の第7分節で強い発現が見られるようになり、その後の発生ステージでは、中枢神経および眼のほかに鰓弓の周辺・体節などさまざまな組織で発現が見られた(図2)。オタマジャクシの脳では、終脳(大脳)・間脳の一部および後脳の各分節での発現が見られた。本研究ではさらに初期神経胚という神経発生において非常に初期の段階での発現パターンに注目し、UCP2がこの時期に特に重要な役割をもつのではないかと考えて研究を進めている。
これまでのところ、アンチセンスモルフォリノオリゴを用いた翻訳阻害によって初期神経胚においてEn2やKrox20といった領域決定に関わるマーカー遺伝子の発現が減少することがわかった。またmRNAの顕微注入による過剰発現実験でもこれらのマーカー遺伝子の発現が変化するという結果が得られている。
今後、UCP2の翻訳阻害・過剰発現実験においてさらに多くのマーカー遺伝子の変化を観察すると同時に、UCP2がミトコンドリアタンパク質であるという点から考えられる細胞内でのさまざまな生命活動と神経領域の発生との関わりの可能性を探り、UCP2の初期発生における役割を解明したい。
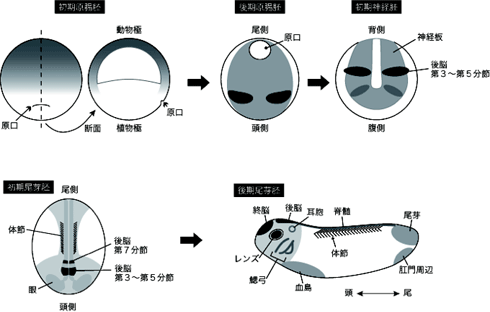
図2 ツメガエル初期胚におけるUCP2の発現パターン
(3)アフリカツメガエル胚発生過程の3次元立体像構築
アフリカツメガエル胚は発生学でよく用いられるモデル生物であるが、その発生過程中は外観がほぼ変わらない。一方、胚内部では細胞群の大移動が起こることで新しい組織や器官が形成されていく。しかしアフリカツメガエル胚は不透明であるため、直接その様子を観察することはできない。また、外観の特徴が少ないにも関わらず、発生の段階を定義するためのステージ基準をそこに求めるため、非常に曖昧で研究者ごとが主観的に決定してしまうという問題がある。特に初期胚では、短期間で内部構造は変化していくので、その期間のステージを用いた実験結果に対して、本当に我々と同じ目線で見たステージなのかが疑わしく思われる。さらに、この外観は必ずしも内部構造と一致していないため、ステージの定義に対する曖昧さは増す。
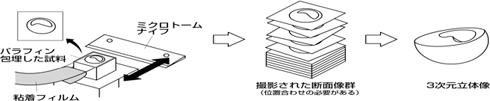
図3 内部構造顕微鏡の原理
これらの問題に対してアフリカツメガエル胚の発生過程をコンピュータ上に再現することで、1)発生時間軸に即した内部構造の形状変化の容易な観察、2)胚の形状をデジタル情報に置き換えることで得られる特徴量を計測してその数値を解析することで、客観的なステージの基準を定義する、ことができるのではないかと考えた。
まずツメガエル胚を3次元立体像化するためにこれまで3次元内部構造顕微鏡(小林ら1995、横田秀夫2004、小川ら2003)を用いて胚の断面像を取得していた(図3)。しかしこの方法は、得られた断面像の補正処理に膨大な時間がかかってしまうため、多数の標本を揃えるのは困難であった。この問題に対し、本年度から連続組織切片粘着フィルム法(川本2002)を導入した。連続組織切片を回収して断面像化することで3次元立体像を構築する方法は以前から試みられていたが(Kaufman et.al. 1998)、切片を破損・変形することなく全て回収することは非常に困難であった。しかしこの方法は、切削断面に特殊な粘着フィルムを貼り付けることで正常に全ての切片を回収することができる。また、パラフィン包埋に比べて、より安定して切片を回収できるように樹脂包埋を用いた。さらに、回収された切片群プレパラートをフィルムスキャナを用いて一度にコンピュータ内に取り込み、画像補正することで非常に短時間で断面像化を取得できるようになった。唯一懸念であった軸の位置合わせはDeltaViewer(和田2007)を用いることで解決された。
このようにして取得された断面像から3次元立体像を構築し、そのままの状態では包埋時の胚一つ一つの位置関係がバラバラで正しい計測ができないため、3次元位置補正を行なうソフトウェアをZedView(LEXI Co., Ltd.)をベースに開発した。その結果、位置関係が一定の3次元立体像を構築できた(図4)。
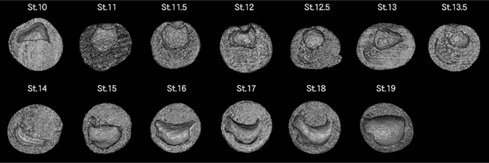
図3 アフリカツメガエルの3次元立体像(縦断面)
3次元立体像からは表1に示す計45箇所の計測を行ない、得られた数値をそのステージの形状を表す特徴量として捉えた。さらに、計測値はそのまま利用すると個体形状によってばらつきが生じるため、長さや体積などの比率をとって解析を行なった。今回は得られた計測値群をグループ分けすることができる判別分析を行なってステージ判別の指標とした(表1)。また、今回の解析用にPV-WAVE(Visual Numerics Inc.)をベースにしステージ判別用のソフトウェアの開発を行なった。

その結果、表2のような各ステージ区間を判定するための数式が得られた。
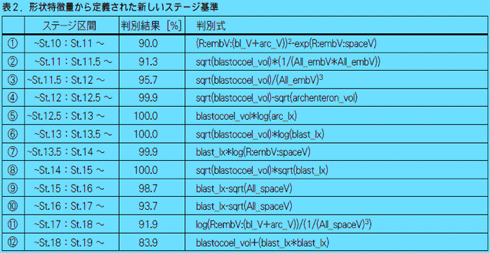
以上の結果から、これまでは一つ一つ切ってみなければわからなかったアフリカツメガエル胚をコンピュータ内で再現し、自由に内部構造を時系列に沿って観察することができるモデルを構築することができた。また、得られた3次元立体像を数値に置き換えて解析することで目視による外観情報に頼らない新しいステージ決定基準を示唆することができた。
今後は、回収された切片に対してin situハイブリダイゼーションを行ない、遺伝子発現の3次元立体像をこのモデルに添加することで、様々な遺伝子発現の時間的・空間的な位置関係を示すことも可能となる。
おわりに
ここまで脊椎動物の体づくりの仕組みを、ツメガエルを用いた解析結果として簡単にご紹介したが、今年度新たに開始したプロジェクトであるイモリとツメガエルの比較解析についても簡単に述べておく。両生類の原腸形成過程は古くから解析が進められており、現在ではほぼ確立していると考えられている。したがって、分子生物学的解析を行ないやすいツメガエルと実験発生学的解析を行ないやすいイモリなどとその役割分担がなされ研究が進んできた。しかし我々の解析によって、ツメガエルとイモリでは体軸を伸ばす方向から神経誘導の時期や頭部形成の機構まで正反対と言っても過言ではないくらいに異なっていることが分かって来た。また、これらの違いはそれぞれがその他の脊椎動物種の特徴を含んでおり、結果としてイモリとツメガエルの比較によって脊椎動物に潜む原腸形成過程の普遍性を知る1つの方法になる可能性が示唆された。今後は遺伝子発現の解析や基地の遺伝子の働きを調べ、また実験発生学的方法論を駆使することで、イモリとツメガエルの本質的な相違点と相同点を見いだして行き、その中にこれまでに分かった神経堤やプラコードの形成機構に関する成果などを当てはめて脊椎動物の形態(ゲノム)が包含する進化的な意味について考察して行きたい。
参考文献
1) Besson A, Dowdy SF and Roberts JM (2008) CDK inhibitors: cell cycle regulators and beyond. Dev Cell 14;159-169
2) Besson A, Dowdy SF and Roberts JM (2008) CDK inhibitors: cell cycle regulators and beyond. Dev Cell 14:159-169
3) Nagatomo K and Hashimoto C (2007) Xenopus hairy2 functions in neural crest formation by maintaining cells in a mitotic and undifferentiated state. Dev Dyn 236:1475-1483
4) Schlosser G (2005) Evolutionary origins of vertebrate placodes: insights from developmental studies and from comparisons with other deuterostomes. J Exp Zoolog B Mol
Dev Evol 304:347-399
5) Schlosser G (2008) Do vertebrate neural crest and cranial placodes have a common evolutionary origin? Bioessays 30:659-672
6) Streit A (2004) Early development of the cranial sensory nervous system: from a common field to individual placodes. Dev Biol 276:1-15
7) ernon AE, Devine C and Philpott A (2003) The cdk inhibitor p27Xic1 is required for differentiation of primary neurones in Xenopus. Development 130:85-92
8) Joseph JW, Koshkin V, Saleh MC, Sivitz WI, Zhang C-Y, Lowell BB, Chan CB and Wheeler MB (2004) Free Fatty Acid-induced -Cell Defects Are Dependent on Uncoupling
Protein 2 Expression. J Biol Chem 279:51049-51056.
9) Negre-Salvayre A, Hirtz C, Carrera G, Cazenave R, Troly M, Salvayre R, Penicaud L and Casteilla L (1997) A role for uncoupoing protein-2 as a regulator of
mitochondrial hydrogen peroxide generation. The FASEB Journal 11:809-815.
10) Sasai Y (2001) Roles of Sox factors in neural determination: conserved signaling in evolution? Int J Dev Biol 45:321-326.
11) Wigle J and Eisenstat D (2008) Homeobox genes in vertebrate forebrain development and disease. Clin Genet 73:212-226.
12) 小林、樋口、青木、工藤 (1995) 「三次元内部構造顕微鏡の開発」 精密工学会誌, 第61巻, 第1号, 100-106
13) 横田秀夫(2004)「生体を対象としたディジタイジングのための三次元内部構造顕微鏡の開発」 生体力学シミュレーション研究プロジェクト第一期成果報告会予稿
14) 川,宮下,清水,杉山(2003) 「連続切片の自家蛍光観察によるダイズ種子の3次元内部構造」 日本食品科学工学会誌 Vol.50, No.5, 213-217
15) 本忠文(2002)「粘着フィルム法による多目的新鮮凍結切片の作製と応用実験」 病理組織技術研究会誌,11:1-18
16) Kaufman MH., Brune RM., Davidson DR and Baldock RA. (1998). Computer-generated three-dimensional reconstructions of serially sectioned mouse embryos. J Anat.
193:323-36.
17) 和田 昌昭, 「DeltaViewerによる連続切片からの3D構築」比較生理生化学. 24: 160-165 (2007).
