年度別活動報告
年度別活動報告書:2011年度
脊索動物と節足動物の共通祖先を理解する 2−2 カドヘリンの構造と機能の解析
小田広樹(主任研究員) 秋山-小田康子(特別研究員)
佐々木瑞希(奨励研究員) 野田彰子(研究補助員)
西口茂孝(大阪大学大学院生)
はじめに
多細胞動物は、細胞と細胞を連結する微細構造(ジャンクションと呼ぶ)を持ち、ジャンクションを巧みに操ることによって体の形を作り上げる。ジャンクションには何種類かのタイプが知られており、その中でアドヘレンスジャンクションは多細胞動物に普遍的に見られるジャンクションで、形態形成に最も密接に関わっていることが知られている7)。アドヘレンスジャンクションの主要な接着分子はクラシカルカドヘリン(以後、カドヘリンと呼ぶ)である。このカドヘリンは隣接した細胞に発現する同種のカドヘリンを認識し、結合する。細胞間隙で起こる、この同種カドヘリン間の結合は、細胞外カドヘリンドメイン(EC)と呼ばれる繰り返し構造を介して達成されているが、カドヘリンのECドメインの数や細胞外領域のドメイン構成には、多細胞動物の系統間で多様性がある。カドヘリンの構造はどのように多様化してきたのか。その際、ジャンクションにおける接着の仕組みは変化したのか。さらに、そのようなジャンクションの変化は形態形成の仕組みに影響を与えなかったのか。本研究では、これらの疑問に対する答えを探究したいと考えている。
これまでの比較解析では、その構造的多様性がヒトデやクモで共通に見られる状態からの独立的な短縮化で説明できることを見いだしている8) 9)。短縮化されたひとつの状態である“昆虫型”は7個のECドメインを持ち、少なくともハエ、コオロギ、トビムシ、アルテミアで共通であり、それとは別の状態として、5個のECドメインを持つ“脊椎型”が脊椎動物とホヤで共通に存在する。ここで注目すべきは、脊椎型カドヘリンの5個のECドメインと昆虫型カドヘリンの7個のECドメインは異なる起源を持つ点である。これまで細胞間接着の構造的仕組みは脊椎型のカドヘリンを使って詳細に解析されてきており、脊椎型のカドヘリンでは細胞膜から最も遠位の2つのECドメイン(EC1とEC2)がホモフィリックな接着に主要な役割を果たしていることが知られている。そして、その2つのECドメインのうちEC1内の配列のわずかな違いが接着特異性を決めていることも分かっている。一方、ショウジョウバエのDEカドヘリンの解析では、このカドヘリンの7つのECドメインのうち、細胞膜から遠位の6個のECドメイン(EC1-EC6)が存在すれば強い接着活性が得られることが明らかになっている10)。しかし、ホモフィリックな接着において、その6個のECドメインがそれぞれどのような役割を果たしているかは全く不明である。そこで私たちは、昨年度、キイロショウジョウバエ (Drosophila melanogaster) のDEカドヘリンとフタホシコオロギ (Gryllus bimaculatus) のGbEカドヘリンが異なる接着特異性を示すことを利用して、昆虫型Eカドヘリンの接着メカニズムを解析する試みを始めた。今年度は、様々にデザインしたキメラ分子の解析から、EC2からEC4が昆虫型カドヘリン接着の種特異性を決める構造的仕組みに重要であることが分かった。
結果と考察
DEカドヘリンとGbEカドヘリンのキメラ分子の作製と細胞集合実験
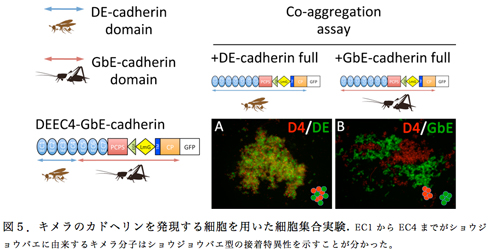
DEカドヘリンとGbEカドヘリンのキメラ分子を様々な部位で切り替えて作製し、それらのキメラ分子を発現させた培養細胞を用いて集合実験を行うことによって、作製したそれぞれのキメラ分子がDEカドヘリンの接着特異性をもつか、GbEカドヘリンの接着特異性をもつかを調査した(図5)。その結果、EC1だけを別の動物種由来のものに置き換えても接着特異性は変わらなかったが、EC1からEC4までを置き換えると接着特異性が変わった。この結果は、EC2からEC4までの間に接着の種特異性に関わる領域が存在することを示唆した。ところが、EC2とEC3だけを別種の動物由来にしたキメラ分子では接着特異性が失われ、どちらの動物種のカドヘリンに対しても結合活性を示すようになった。これらの結果を総合すると、EC4に昆虫型Eカドヘリンの接着特異性を決める仕組みに関わる領域があることが考えられた。しかし、なぜEC2-EC3領域の置き換えで接着特異性が失われたのかは理解が難しい。このことは昆虫型カドヘリンによる接着の構造的仕組みがそんなに単純ではないことを示唆しているのかもしれないが、様々な組み合わせでキメラ分子の活性を比較解析することによって、その仕組みに関してより詳細な理解が得られると期待している。
おわりに
今年度の研究により、脊椎型のカドヘリンと昆虫型のカドヘリンではホモフィリックな接着のための構造的仕組みにいくらかの違いが存在することが推察された。カドヘリンによる細胞間接着は多細胞動物にとって普遍的に重要な機能であるにもかかわらず、その分子の構造は系統によって独自の進化を遂げている可能性がある。今後の研究で、そのような接着構造の進化が形態形成の進化と関連付けられるとおもしろいと考えている。
引用文献
- 1) Akiyama-Oda, Y., Oda, H. (2010) Cell migration that orients the dorsoventral axis is coordinated with anteroposterior patterning mediated by Hedgehog signaling in the early spider embryo. Development 137, 1263-1273.
- 2) Nüsslein-Volhard, C., Wieschaus, E. (1980) Mutations affecting segment number and polarity in Drosophila. Nature 287, 795-801.
- 3) Driever, W., Nüsslein-Volhard, C. (1988) The bicoid protein determines position in the Drosophila embryo in a concentration-dependent manner. Cell 54, 95-104.
- 4) Stauber, M., Jäckle, H., Schmidt-Ott, U. (1999) The anterior determinant bicoid of Drosophila is a derived Hox class 3 gene. Proc. Natl. Acad. Sci. U.S.A. 96, 3786-3789.
- 5) Yazawa, S., Umesono, Y., Hayashi, T., Tarui, H., and Agata, K. (2009) Planarian Hedgehog/Patched establishes anterior-posterior polarity by regulating Wnt signaling. Proc. Natl. Acad. Sci. U.S.A. 106:52, 22329-34.
- 6) Kanayama, M., Akiyama-Oda, Y., Nishimura, O., Tarui, H., Agata, K., and Oda, H. (2011) Travelling and splitting of a wave of hedgehog expression involved in spider-head segmentation. Nature Communications 2, 500.
- 7) Gumbiner, B.M. (2005) Regulation of cadherin-mediated adhesion in morphogenesis. Nat. Rev. Mol. Cell Biol. 6, 622-634.
- 8) Oda, H., Tagawa, K., Akiyama-Oda, Y. (2005) Diversification of epithelial adherens junctions with independent reductive changes in cadherin form: identification of potential molecular synapomorphies among bilaterians. Evol. Dev. 7, 376-389.
- 9) Oda, H., and Takeichi, M. (2011) Structural and functional diversity of cadherin at the adherens junction. Journal of Cell Biology 193, 1137-1146.
- 10) Haruta, T., Warrior, R., Yonemura, S., Oda, H. (2010) The proximal half of the Drosophila E-cadherin extracellular region is dispensable for many cadherin-dependent events but required for ventral furrow formation. Genes Cells 15, 193-208.
