年度別活動報告
年度別活動報告書:2005年度
アゲハチョウの食草選択と進化
尾崎克久(研究員)
中山忠宣(奨励研究員)
廣崎由利恵(研究補助員)
山田歩(大学院生)
Yann SALAHUN(研修生)
吉川寛(顧問)
はじめに
あらゆる生物が、他の生物と何らかの関わり合いを持ちながら棲息している。相互作用は様々な形で種間にも個体間にも存在し、長い進化の歴史の中で洗練された、巧妙な仕組みによって成り立っている。現在、多くの生物種のゲノム解読が進行しており、生物に関する飛躍的な理解の向上が進んでいる。生物の巧みな生活史戦略や生存の様子を理解するには、ゲノムの情報を基盤として様々な角度からの情報の蓄積が必要である。生物間相互作用に関する仕組みを解明する試みは、ゲノム塩基配列解読後の生物学において最も重要な課題の一つである。
生物間のコミュニケーションの多くは、化合物を介して行われている。植物は自らの生命維持には直結しない、様々な化合物を体内で生産している(二次代謝物質)。二次代謝物質の組み合わせは植物種ごとに異なっており、植食性昆虫にとっては食草を識別するための重要な手がかりとなっている。アゲハチョウの仲間は、他の多くの植食性昆虫と同様に、特定の植物のみを餌として利用する。卵から孵化したばかりの幼虫は、体が小さく移動能力が低いため、自力で餌を探索することは困難である。このため、メス成虫による正確な植物種の識別と産卵場所の選択は、次世代の生存を左右する重要な役割である。メス成虫は産卵の直前に前脚で葉に触れることで含有する化合物を感じ取り、その組み合わせによって産卵行動が引き起こされる。ナミアゲハ(Papilio xuthus)では、ウンシュウミカンの葉から産卵刺激物質として10種類の化合物が単離されている 1)。それらは、主としてフラボノイド、アミン類、糖の誘導体に分類される。他にも数種のアゲハ類で産卵刺激物質が明らかにされており、これらの構造についてアゲハ種間で比較すると類似性が認められる。植物の系統的近縁性とは無関係に、植物に含まれている化合物の類似性が寄主転換の可能性を支え、食性の進化を可能にしたのではないかと考えられている 2)。これまでに報告されている産卵刺激物質は全て不揮発性であるため、アゲハチョウは「味」のようなものとして認識していると考えられている。前脚で味を感じる仕組みの解明は、昆虫の多様化における食草転換という生命現象の適応的意義を理解する手がかりとなる。
産卵刺激物質を認識する前脚ふ節には、化学感覚毛と呼ばれる特殊な器官が多数存在する。化学感覚毛の構造はショウジョウバエの典型的な味覚組織に類似し、味覚ニューロンが存在することから、産卵刺激物質を受容する味覚レセプターを発現していると考えられる。ミカン科食性のアゲハチョウ間であっても、種ごとに産卵刺激物質として認識する化合物の組み合わせが異なるため、種ごとに特徴的な多様な味覚レセプターを持っていることが予測される。また、味覚レセプターが化合物を認識するためには、化合物が化学感覚毛内のリンパ液を通り抜けてレセプターに到達する必要があるため、化合物を結合して運搬する役割を持つタンパクが必要になるであろう。味覚レセプターと化合物結合タンパクを中心とする産卵刺激物質受容システムに関わる遺伝子群を解明し、複数種間で比較することができれば、昆虫と植物を強固に結びつけている仕組みを解明し、生物間相互作用を理解する手がかりが得られると考えた。
昆虫の味覚に関する研究が本格的に始まったのは20年以上前に遡るが 3)、味覚レセプターは2000年になって初めて7回膜貫通Gタンパク質共役型レセプター(以下GPCRと略)が報告された 4)。化学受容のGPCRは一次構造の多様性が高く、脊椎動物から報告されている味覚・嗅覚のGPCRとの類似性を手がかりとした探索は困難であり、ショウジョウバエの全ゲノム配列の情報科学的解析によって候補遺伝子ファミリーが同定された。昆虫の味覚レセプターは極端に発現量が少ないため解析は困難を極め、直接的な証拠によって機能が解明されているものはまだ一つだけである 5)。化合物結合タンパクについて、味覚での機能に関する報告はまだないものの、味覚器官で発現するものが見つかっている 6)。また、多種昆虫から化合物結合タンパクの遺伝子が報告され、情報が蓄積しつつある。
本研究は、主たる食草の産卵刺激物質が明らかにされているナミアゲハとシロオビアゲハを材料として用い、メス成虫前脚ふ節に発現する味覚レセプター遺伝子及び化合物結合タンパク遺伝子をクローニングし、その機能と特徴の解明を目的として取り組んでいる。初年度(2001年)はナミアゲハメス成虫前脚ふ節からcDNAライブラリーを調製し、大量塩基配列決定法とRT-PCRによる発現部位決定法を確立した。2002年度はナミアゲハのメス成虫前脚ふ節cDNAライブラリーの網羅的な塩基配列決定及び、得られた配列の情報解析、発現解析を行った。その結果、ふ節に特異的に発現する味覚タイプのGPCRであるPXFT-01989、化学感覚器官に限定的に発現する3種類の化合物結合タンパク(chemosensory protein: CSP)、ふ節で発現する3種のアミンレセプター及び1種類のチトクロームp450の遺伝子をクローニングした 7)。2003年度はFosmidベクターを用いてナミアゲハゲノムライブラリーを作製し、既に得られた上記候補遺伝子をプローブとして、ゲノム上の遺伝子の全構造と関連遺伝子ファミリーのクローニングを行った。2004年度は、ふ節に特異的に発現する味覚タイプGPCR遺伝子であるPXFT-01989から、選択的スプライシングによって少なくとも4種類のメッセンジャーRNAが作られていることを発見した。また、PXFT-01989遺伝子を手がかりとして、他のアゲハチョウからGPCR遺伝子を探索した結果、シロオビアゲハから類似性の高い部分配列を発見した。複数のGPCR遺伝子の発見を目的として、シロオビアゲハのメス成虫ふ節の完全長cDNAライブラリーを作成した。
今年度は、バキュロウイルスベクターを用いて培養昆虫細胞中でPXFT-01989遺伝子を発現させ、カルシウムイメージング法を用いて化合物への応答について解析を行った。また、シロオビアゲハのcDNAライブラリーについて網羅的に塩基配列を決定し、ナミアゲハのcDNAライブラリーとの比較を行った。シロオビアゲハのcDNAライブラリーからも化合物結合タンパクの遺伝子を多数発見し、CSPファミリーについてナミアゲハと比較することでこの遺伝子ファミリーの進化について考察した。
GPCRの機能解析
ショウジョウバエの化学受容GPCRは、アミノ酸配列の特徴などから味覚ファミリー(Gr)と嗅覚ファミリー(Or)に分けられる。ナミアゲハGPCR・PXFT-01989は、アミノ酸配列の類似性から味覚ファミリーに属すると考えられる。このGPCRが認識する化合物(リガンド)を特定するため、外部からの刺激に対する細胞内のカルシウム濃度の変化を観察する「カルシウム・イメージング法」を用いた解析を試みた。その方法は、培養昆虫細胞にバキュロウイルスを利用してPXFT-01989遺伝子を導入し、本来はこの遺伝子を持たない細胞中で強制的に発現させた。ナミアゲハの味覚タイプGPCR遺伝子・PXFT-01989を組み込んだバキュロウイルス発現ベクターと、発光クラゲの発光遺伝子Aequorin(エコーリン)を組み込んだバキュロウイルス発現ベクターを作成し、培養昆虫細胞Sf9に感染させた。Aequorinはカルシウム依存的に発光するため、GPCRと同時に感染させた細胞をリガンドで刺激すると、細胞内カルシウム濃度の上昇を発光として検出できる。このような解析手法を「カルシウム・イメージング法」という。本研究では、カルシウム応答の詳細な解析を行うことを目的とし、独自に装置を改造して最大5種類の化合物で連続刺激が行えるようにしている。さらに、化合物溶液が短時間で培養昆虫細胞のディッシュ内に広がり、短時間で排出されるように刺激方法を工夫している。
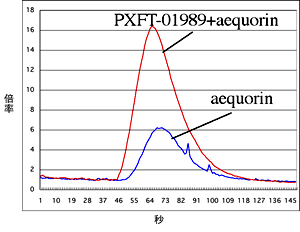
細胞:ウイルス粒子の比を1:0.5(MOI 0.5)に調製してバキュロウイルスを感染させた培養昆虫細胞では、感染から96時間後から114時間後の間に最も強い発光が観察された。培養昆虫細胞を試験区用(PXFT-01989とAequoeinを同時に発現)と比較対照区用(Aequorinのみを発現)に分注し、感染させるウイルスの種類を変更するだけで異なる結果が得られるため、試験区と比較対照区の細胞の条件をそろえることが容易であり、感染後の時間に応じて安定した結果が得られた。ミカンの葉から抽出した混合化合物0.01%濃度で細胞の刺激を行った場合、Aequorinみのを発現させた細胞でも発光が観察されたが、PXFT-01989とAequrinを同時に発現させた細胞では明らかに強い発光が観察された(図1)。
|
|
図1 ミカンの葉抽出物0.01%での刺激
PXFT-01989を発現させた細胞では、aequorinのみを発現させた細胞より明らかに強い反応が見られた
この結果は、PXFT-01989がミカンの葉から抽出された化合物のいずれかをリガンドとして認識し、細胞内のカルシウム濃度を上昇させたと考えられる。ナミアゲハの産卵刺激物質として報告されている化合物のうち、購入または合成により入手可能な9種類について、単一化合物による刺激を同様に行った結果、Synephrine(シネフリン)でのみ上記の混合化合物と同様の結果が得られた(図2)。
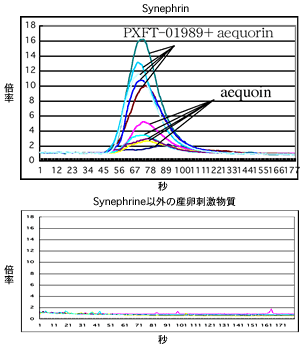 |
図2 Synephrine 250uMでの刺激
ミカンの葉抽出物と同様に、PXFT-01989を発現させた細胞で明らかに強い反応が観察された。
この結果から、PXFT-01989がSynephrineをリガンドとして認識し、細胞内のカルシウム濃度を上昇させたと考えられる。ミカンの葉から抽出した混合化合物で刺激した場合と同様の結果であったことから、PXFT-01989が混合化合物に含まれるSynephrineに反応していたのではないかと考えられる。培養昆虫細胞Sf9には内在性のOctopamine(オクトパミン)レセプターの存在が知られている。SynephrineはOctopamineと構造がよく似たアミン類の一種であり、Octopamineレセプターの作用物質として機能することが知られている 8)。観察された発光が内在性Octopamineレセプターによる反応である可能性があるので、同じ濃度のOctopamineによる刺激を試みた。その結果、PXFT-01989とAequorinを同時に発現する細胞と、Aequorinのみを発現する細胞で差がなかった(図3)。
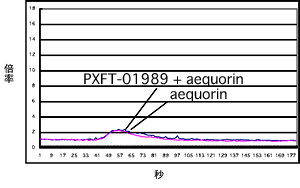 |
図3 Octopamine 250uMでの刺激
Synephrineで刺激を行った場合の様な、反応の違いは観察されなかった。
Synephrineと構造が似た別の6種類の化合物(図4)でも同様に刺激を行ったが、発光は観察されなかった。この結果から、PXFT-01989はSynephrineに高い特異性を示すレセプターであると考えられる。
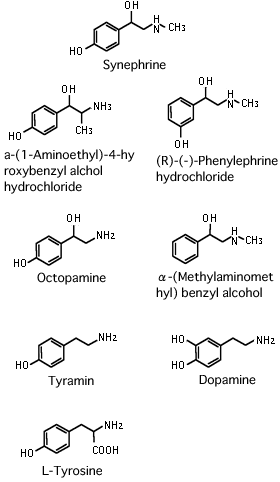 |
図4 Synephrine 関連化合物の構造図
シロオビアゲハのcDNAライブラリー
すでに2002年度に報告しているナミアゲハふ節cDNAライブラリに続いて、今年度はシロオビアゲハふ節cDNAライブラリの構築と解析を行った。羽化翌日の未交尾雌成虫20個体から前脚ふ節40本を単離、全RNAを抽出し、シロオビアゲハふ節全長cDNAライブラリを構築した。ライブラリサイズは約2×105クローンで、そのうち約15,000クローンについて両方向から塩基配列を決定した。
得られた配列をアセンブルした結果、3,503種類の配列にまとめることができた。クローンの数に比べて配列の種類数が少ないのは、同じcDNA配列が重複してライブラリに含まれているためである。配列の重複度(Redundancy)は、この組織においての遺伝子の発現量を反映する。約70%の配列について重複度が1であったことから、このcDNAライブラリが組織で発現する多様な遺伝子を含んでいると考えられる。この3,503種類のcDNA配列を、NCBIに登録されている遺伝子と比較(BLASTX-search)したところ、約2,000個の配列について相同な遺伝子を発見した。そのうち、NCBIのデータベース情報から機能を推定できたものが、740種類あった。
これらの配列を予測された機能ごとにグループ分けしたところ、酸化還元酵素、細胞骨格、タンパク質合成などの『House-keeping gene(細胞維持に必要な遺伝子)』が約60%を占めていた(図5)。残りは、おもに「Odorant & other ligand binding protein」と「Receptor, Channel, Transporter etc. 」に分類され、この2グループの遺伝子の存在が、ふ節という化学感覚器官を特徴づけていると言える結果となった。
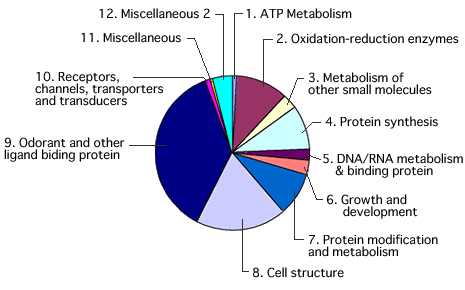 |
図5 cDNAライブラリーからみつかった遺伝子の種類
リガンドを結合し、運搬する機能を持つと考えられている遺伝子群が最大のグループとなった。
化合物結合タンパク(CSP)の比較
「Odorant & other ligand binding protein」のグループは、機能の予測できたcDNA配列のうち36%を占め、Redundancy = 700という最も重複度の高い配列を含んでいた。我々は、このグループからCSP (Chemosensory Protein)やOBP (Odorant Binding Protein)の相同遺伝子と思われる配列を発見し、各配列のORF(Open Reading Frame)を推定、アミノ酸配列に変換した。アミノ酸配列を整理したところ、シロオビアゲハcDNAライブラリには、13種類のCSP遺伝子が含まれていることがわかった。これまでに、ナミアゲハのcDNAライブラリからは11種類のCSPが、ゲノムライブラリからはさらに8種類のCSPが発見されている(2002年度報告書参照)ため、今回発見したシロオビアゲハのCSP13種類と比較した。
CSPは、低分子量(10~15kDa)の分泌タンパク質で、昆虫から特に多く発見されている。CSPは主に化学感覚毛のリンパ液中に存在し、その他には分泌細胞など全身各所での発現が確認されている。これまでに様々な研究が行われてきたが、生体内におけるCSPの機能は未解明である。しかしその中で、2002年にLartigueらがヨトウガCSPの立体構造を解析し、化合物との結合の様子を考察している。その後、ハチやアリの仲間やガの仲間でも、触角などの化学感覚器官からCSPが発見されてきた。
以上の知見から、CSPは化合物(リガンド)と結合し、その化合物を神経細胞膜上の受容体まで運ぶ「運搬タンパク質」や、受容体に結合した化合物を代謝する「分解タンパク質」として機能しているのではないかと考えられている。アゲハチョウの前脚ふ節において多様なCSPやOBPのcDNAが発見される事実は、これらのタンパク質がふ節で何らかの機能を発揮していることを示唆する。アゲハチョウのCSPやOBPが食草認識のシステムに関わっているのか否か、このタンパク質群の機能を解明することで明らかにしていくことを目指し、今年度はその前段階として、ナミアゲハとシロオビアゲハのCSPについて比較解析を行った。
化合物結合タンパク(CSP)の比較
「Odorant & other ligand binding protein」のグループは、機能の予測できたcDNA配列のうち36%を占め、Redundancy = 700という最も重複度の高い配列を含んでいた。我々は、このグループからCSP (Chemosensory Protein)やOBP (Odorant Binding Protein)の相同遺伝子と思われる配列を発見し、各配列のORF(Open Reading Frame)を推定、アミノ酸配列に変換した。アミノ酸配列を整理したところ、シロオビアゲハcDNAライブラリには、13種類のCSP遺伝子が含まれていることがわかった。これまでに、ナミアゲハのcDNAライブラリからは11種類のCSPが、ゲノムライブラリからはさらに8種類のCSPが発見されている(2002年度報告書参照)ため、今回発見したシロオビアゲハのCSP13種類と比較した。
CSPは、低分子量(10~15kDa)の分泌タンパク質で、昆虫から特に多く発見されている。CSPは主に化学感覚毛のリンパ液中に存在し、その他には分泌細胞など全身各所での発現が確認されている。これまでに様々な研究が行われてきたが、生体内におけるCSPの機能は未解明である。しかしその中で、2002年にLartigueらがヨトウガCSPの立体構造を解析し、化合物との結合の様子を考察している。その後、ハチやアリの仲間やガの仲間でも、触角などの化学感覚器官からCSPが発見されてきた。
以上の知見から、CSPは化合物(リガンド)と結合し、その化合物を神経細胞膜上の受容体まで運ぶ「運搬タンパク質」や、受容体に結合した化合物を代謝する「分解タンパク質」として機能しているのではないかと考えられている。アゲハチョウの前脚ふ節において多様なCSPやOBPのcDNAが発見される事実は、これらのタンパク質がふ節で何らかの機能を発揮していることを示唆する。アゲハチョウのCSPやOBPが食草認識のシステムに関わっているのか否か、このタンパク質群の機能を解明することで明らかにしていくことを目指し、今年度はその前段階として、ナミアゲハとシロオビアゲハのCSPについて比較解析を行った。
アゲハチョウ科におけるCSP群の比較解析
すでに発見している19種類のナミアゲハCSPと、今回cDNAライブラリから同定した13種類のシロオビアゲハCSPについて、塩基配列を比較した(BLASTN)。その結果、この2種のアゲハチョウで、対(ペア)となるCSPを11組発見した。ペアになるCSP同士の相同性が高く(アミノ酸配列平均86%一致)、その一方で異なるペアに属するCSP同士は相同性が低かった(アミノ酸配列平均36%一致)。これは、ナミアゲハとシロオビアゲハが分岐する以前に、すでにCSPは多様化をしていたことを示唆する。
さらに、11組のペアを作ったCSPについて、ペアのCSPの間にどのような塩基置換が生じているのか解析した。すると、同義置換の割合はペア間でほぼ一定(5~10%)に保たれているのに対して、非同義置換(アミノ酸置換につながる塩基置換)の割合は5~27%まで多様性があった。この違いは、『非同義置換と同義置換の比』をとることで、より明確になる(図6)。CSP1,2,4は非同義置換の割合が小さく、ナミアゲハとシロオビアゲハでよく保存されているといえる。逆にCSP8bは、非同義置換の割合が大きい。
ナミアゲハでのゲノム構造の解析から、CSPファミリーはゲノム上でクラスターを形成していることがわかっている。このクラスターの中には、相同性の高い遺伝子が連続して存在する部分があり、CSPはゲノム上の重複によってファミリーの数を増やし多様化してきたのではないかと考えられる。また、このグループの中に、よく保存されているCSP(CSP1)とよく変化しているCSP(CSP8,8b)が存在することから、CSP1のような保存性の高いCSPは2種のチョウで類似の機能を担い、CSP8や8bのように変化の大きいCSPは2種のチョウの生理的な違いに関係しているという仮説が考えられる。
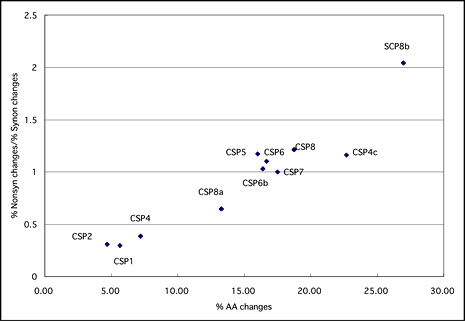 |
図6 アミノ酸置換率に対する非同義置換と同義置換の比率
ナミアゲハでのゲノム構造の解析から、CSPファミリーは染色体上でクラスターを形成していることがわかっている。このクラスターの中には、相同性の高い遺伝子が連続して存在する部分があり、CSPは染色体上の重複によってファミリーの数を増やし多様化してきたのではないかと考えられる。また、このグループの中に、よく保存されているCSP(CSP1, 2, 4)とよく変化しているCSP(CSP8b)が存在する様子から、CSP1のような保存性の高いCSPは2種のチョウで類似の機能を担い、CSP 8bのように変化の大きいCSPは2種のチョウの多様化に寄与しているという仮説が考えられる。
おわりに
より詳細な解析を必要とする部分を残しつつも、ナミアゲハの味覚タイプGPCR、PXFT-01989が産卵刺激物質の一つであるSynephrineを特異的に受容することが明らかになった。研究例の多いショウジョウバエでもリガンドが特定されている味覚レセプターは一つしかない中、モデル生物ではないナミアゲハから産卵行動という重要な生命現象に関わるレセプターを発見できたことは特筆に値すると思われる。
シロオビアゲハのcDNAライブラリーの解析においては、約半年で15,000クローンの塩基配列を両方向から決定できたことは、研究施設の規模を考えると大変な早さである。そこから大量の遺伝子の情報が検出され、ナミアゲハのcDNAライブラリーと大規模な比較が可能になったことから、大きな成果の一つと言える。特に、CSP遺伝子ファミリーの比較により、進化の過程でゲノム上に起きたイベントの一部を推定することが可能になった。
ミカン科食性のアゲハチョウは、産卵刺激物質として認識される化合物の一部は共通であるが、大部分は種ごとに異なっている。このような多様性は産卵刺激物質受容システムの多様性に由来すると考えられる。また、キアゲハはナミアゲハと雑種交配が可能なほど近縁でありながら、食性は異なっている。食性の変化も産卵刺激物質受容システムの多様化と深い関わりがあると考えられるので、このシステムに関与する遺伝子群を数種の近縁種から同定し比較することで、種分化のメカニズムの解明に迫りたいと考えている。
参考文献
1 Nishida R, Ohsugi T, Kokubo S, and Fukami H. (1987) Oviposition stimulants of a Citrus-feeding swallowtail butterfly, Papilio xuthus L. Experientia 43:342-344.
2 Feeny, P. (1995) Ecological opportunism and chemical constraints on the host associations of swallowtail butterflies, pp. 9-15. in J. M. Scriber, Y. Tsubaki, and R. C. Lederhouse (eds.). Swallowtail Butterflies: Their Ecology and Evolutionary Biology. Scientific Publishers, Gainesville, Florida.
3 Tanimura, T., Isono, K., Takamura, T., and Shimada, I. (1982). Genetic dimorphism in the taste sensitivity to trehalose in Drosophila melanogaster. J. Comp. Physiol. 141, 433-437.
4 Clyne PJ, Warr CG, Carlson JR. (2000) Candidate taste receptors in Drosophila. Science.287:1830-1834.
5 Chyb, S., Dahanukar, A., Wickens, A., and Carlson, J.R. (2003). Drosophila Gr5a encodes a taste receptor tuned to trehalose. Proc. Natl. Acad. Sci. USA 100 (Suppl 2), 14526-14530.
6 Galindo K, Smith DP. (2001) A large family of divergent Drosophila odorant-binding proteins expressed in gustatory and olfactory sensilla. Genetics. 159:1059-1072.
7 Ono H, Yoshikawa H. (2004) Identification of amine receptors from a swallowtail butterfly, Papilio xuthus L.; cloning and mRNA localization in foreleg chemosensory organ for recognition of host plants. Insect. Biochem. Mol. Biol., 34, 1247-1256.
8 Park JH, Keeley LL. (1998) The Effect of Biogenic Amines and Their Analogs on Carbohydrate Metabolism in the Fat Body of the Cockroach Blaberus discoidalis. General and Comparative Endocrinology 110, 88-95.